I tuoi occhi

Malattie oculari
Esoftalmo
Cos’è?
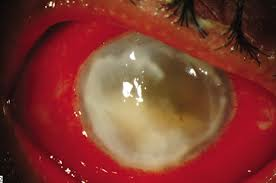
È una condizione in cui l’occhio (bulbo oculare) diventa sporgente rispetto alla sua normale posizione (ossia protrude). L’esoftalmo si distingue dalla proptosi (quando il bulbo è spinto in avanti e in basso); quest’ultima interessa, perlopiù, un solo occhio ed è causata generalmente da processi proliferativi all’interno dell’orbita (tumore orbitale, emorragia retrobulbare, patologie vascolari, ecc.).
Esiste, inoltre, uno “pseudoesoftalmo” caratterizzato da una protrusione del bulbo, causato dall’aumento della lunghezza dello stesso; per esempio nella miopia elevata, e nel glaucoma congenito con buftalmo (occhio grande e sporgente), oppure può svilupparsi dopo numerosi interventi di indebolimento dei muscoli dell’occhio, finalizzati alla correzione dello strabismo.
Perché l’occhio viene fuori?
L’occhio è situato nell’orbita, formata da pareti ossee che – se integre – non sono in grado di deformarsi; ogni aumento di volume del contenuto orbitario e, quindi, anche del bulbo oculare stesso, fa sì che si abbia uno spostamento del suo contenuto in avanti.
La normale posizione dell’occhio è data dalla sua grandezza, dal volume dell’orbita, dai muscoli extraoculari e dal grasso retro-orbitario. Le variazioni di questi parametri determinano l’esoftalmo quando si ha una protrusione in avanti, mentre si ha l’enoftalmo quando si ha una retrazione del bulbo oculare.
Quali sono i sintomi?
Il lieve esoftalmo non è sintomatico; i primi disturbi si manifestano quando la protrusione in avanti raggiunge una certa entità. I soggetti affetti da esoftalmo possono presentare:
- diplopia (visione doppia), causata da una disfunzione dei muscoli oculari a seguito di stati infiammatori o per un processo di compressione dovuto alla patologia sottostante;
- gonfiore delle palpebre, talvolta accompagnato da una sensazione di pressione o pesantezza intorno agli occhi o all’orbita e concomitante presenza di sintomatologia dolorosa. La dislocazione dell’occhio può essere tale da far sì che le palpebre non abbiano la lunghezza sufficiente a coprire l’occhio, soprattutto nella parte centrale, determinando una cheratiteda esposizione; questo comporta seri danni corneali e congiuntivali, fino a pericolose ulcerazioni che possono compromettere la funzione visiva e provocare forti dolori al paziente;
- secchezza oculare;
- iperemia congiuntivale;
- lacrimazione;
- fotofobia;
- riduzione della motilità oculare.
Quali sono le cause dell’esoftalmo?
Tra le cause dell’esoftalmo riconosciamo tutte le alterazioni che creano un aumento di volume del contenuto orbitario. Si possono classificare in:
- tumorali (crescita di una massa nella cavità orbitaria);
- infiammatorie (l’edema dato dall’infiammazione aumenta il volume dei tessuti), da cause fisiche, infettive o traumatiche;
- alterazioni vascolari come la fistola carotido-cavernosa. Tale alterazione è caratterizzata da un’anomala comunicazione tra la carotide interna (arteria che dal collo si porta all’interno del cranio) e il seno cavernoso (canale venoso che passa attraverso una della ossa craniche); la caratteristica di questo esoftalmo (come pure di quello legato ad un aneurisma del seno cavernoso) è la pulsatilità. La spinta sistolica (quando il cuore si contrae e pompa il sangue) fa sì che un maggior volume di sangue arrivi al seno cavernoso, tale aumento di volume si riflette sulla posizione dell’occhio, che seguirà ritmicamente le pulsazioni del cuore aumentando durante la fase sistolica e diminuendo durante la diastolica (quando il cuore si rilassa).
Lo “pseudotumor orbitario” (infiltrazione e proliferazione di cellule non neoplastiche) può causare l’insorgenza di un esoftalmo nell’arco di 2-3 settimane.
Causa molto frequente dell’esoftalmo è il morbo di Basedow dovuto ad ipertiroidismo. In tale condizione patologica si evidenzia un aumento del volume dei muscoli dell’occhio a causa dell’edema e del grasso retro-orbitario, con conseguente sviluppo di esoftalmo (in genere bilaterale) oltre ad altri segni caratteristici, come l’alterata cinesi palpebrale al movimento degli occhi.
Anche la malattia oculare tiroidea (TED – Thyroid Eye Disease), una malattia infiammatoria autoimmune che colpisce l’occhio e i tessuti adiacenti, può provocare esoftalmo. Nella maggior parte dei casi, la TED si presenta in soggetti con una malattia tiroidea autoimmune (morbo di Basedow o anche tiroidite di Hashimoto), e, a volte, può essere riscontrata anche in soggetti con funzione tiroidea normale.
Come si esegue la diagnosi?
La diagnosi dell’esoftalmo è abbastanza immediata, in quanto il segno caratteristico, ossia la sporgenza oculare, è facilmente riconoscibile, occorre comunque sempre far ricorso ad una anamnesi accurata per valutare l’entità dei sintomi e la presenza di eventuali condizioni preesistenti, come problemi alla tiroide o precedenti traumi agli occhi.
Poi, durante la visita, l’oculista dovrà controllare la motilità oculare, l’acuità visiva, la funzione pupillare, l’ampiezza della fessura interpalpebrale. La misura del grado di esoftalmo si esegue tramite uno strumento specifico chiamato esoftalmometro, in grado di valutare con precisione la sporgenza dell’occhio rispetto allo zigomo. La tomografia computerizzata e la risonanza magnetica consentono di diagnosticare con maggior certezza la presenza dell’esoftalmo e sono indispensabili per la valutazione delle alterazioni anatomiche che lo causano. Qualora non vi siano masse (tumorali, vascolari, ecc.), la causa deve essere ricercata – il più delle volte – in uno scompenso tiroideo (sono pertanto necessari test della funzionalità della tiroide). Di fondamentale importanza è l’ecografia oculare, che consente la valutazione dello stato dei muscoli extraoculari e degli altri tessuti molli orbitari.
Qual è la terapia?
La terapia mira ad eliminare l’alterazione che ha causato l’esoftalmo. È importante garantire sempre una buona idratazione della superficie oculare per evitare che si sviluppi una sofferenza della cornea (rimanendo scoperta dalle palpebre); ciò si ottiene con l’uso quotidiano di sostituti lacrimali (lacrime artificiali) sotto forma di collirio o gel. Tale trattamento mira ad umidificare l’occhio e contenere il più possibile i disagi legati alla malocclusione palpebrale. In caso di disepitelizzazione o cheratite da esposizione, è necessario iniziare prontamente una terapia antibiotica per evitare complicazioni infettive.
È fondamentale controllare la funzionalità del nervo ottico, che potrebbe subire delle compressioni da parte della massa infraorbitaria. Nei soggetti con neuropatia ottica, può essere indicato l’utilizzo di farmaci cortisonici o la radioterapia. Nei casi in cui risulti presente la diplopia, può essere utile la prescrizione temporanea di lenti prismatiche.
Qualora l’esoftalmo dovesse rimanere anche dopo la risoluzione della patologia che lo ha generato si può prendere in considerazione l’intervento definito di “decompressione orbitaria”: consiste nell’aumentare il volume dell’orbita andando a ridurre il volume della parete mediale e di quella inferiore (che formano la scatola orbitaria); tale aumento è relativo al numero di pareti che vengono interessate dal trattamento chirurgico. Rimanendo sempre in ambito chirurgico, spesso occorre intervenire per trattare i casi con strabismo importante o con problematiche palpebrali serie.
Quando è necessaria la decompressione orbitaria?
Soprattutto in caso di patologia tiroidea e, in generale, si deve effettuare l’intervento chirurgico quando si ha una otticopatia rapidamente progressiva, cioè quando la compressione orbitaria crea dei danni al nervo ottico che possono causare la perdita irreversibile della funzionalità visiva. Si tratta di un intervento con molti rischi e complicanze; le più comuni anche se non frequenti sono: risultato inadeguato, anestesia infraorbitaria, possibile fuoriuscita del liquido cerebrospinale, disturbi a carico dei seni paranasali e disallineamento dei bulbi oculari con conseguente diplopia.
Cosa fare in caso di esoftalmo?
L’esoftalmo può essere causato da molteplici fattori il cui approccio è spesso plurispecialistico, così come lo è il suo trattamento. Appena si avverte un cambiamento della posizione degli occhi, che sembrano sporgere verso l’esterno (esoftalmo) o retrocedere verso l’interno (enoftalmo), bisogna subito ricorrere all’oculista, che dovrà approfondire la diagnosi con altri specialisti per determinarne la causa e possibilmente rimuoverla.
Riassumendo: come viene valutato in maniera precisa l’esoftalmo?
L’entità della sporgenza dell’occhio viene misurata in millimetri con un apposito strumento (chiamato “esoftalmometro di Hertel”). Lo strumento viene poggiato sui bordi orbitari esterni e, in questo modo, viene fatta collimare sul piccolo specchio l’immagine degli apici corneali contro una scala millimetrata.
L’esame oftalmologico prevede, inoltre, l’osservazione del malato, che deve essere posto sullo stesso piano dell’osservatore (oculista) per valutare la direzione dell’esoftalmo, la sua unilateralità o bilateralità, la presenza di segni di accompagnamento tipo lo strabismo, la ptosi (abbassamento della palpebra), aspetti anomali delle palpebre (tipo cicatrici, edema) o della congiuntiva (iperemia, dilatazione abnorme dei vasi).
Inoltre, è importante, esaminare, con la palpazione, il bordo orbitario per individuare eventuali masse che spingono il bulbo ed, eventualmente, il carattere pulsante della massa. Ovviamente è necessario eseguire, come anticipato in precedenza, un esame oftalmologico completo, che comprende la misurazione dell’acuità visiva, l’esame del segmento anteriore dell’occhio (per valutare una eventuale sofferenza corneale), l’esame del fondo oculare e la valutazione della motilità oculare.
Scheda informativa a cura della Fondazione Sezione Italiana Agenzia internazionale per la prevenzione della cecità-IAPB Italia Ets
Leggi le condizioni generali di consultazione di questo sito
Pagina pubblicata il 6 novembre 2009. Ultimo aggiornamento: 1 settembre 2025
Ultima revisione scientifica: 1 settembre 2025.
Contatta la Fondazione Sezione Italiana dell’Agenzia internazionale per la prevenzione della cecità-IAPB Italia Ets











Scrivi nel Forum: un medico oculista ti risponderà gratuitamente.