Autorizzato negli Usa un nuovo farmaco iniettabile per distrofie retiniche che coinvolgono mutazioni del gene RPE65, in particolare l’amaurosi congenita di Leber
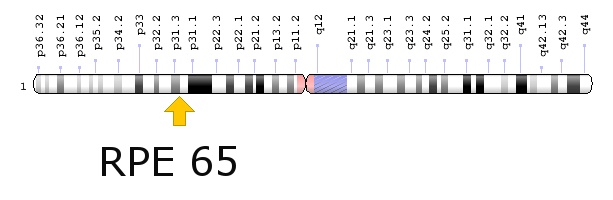
La Food and Drug Administration (FDA), l’Agenzia governativa americana per il farmaco, il 19 dicembre 2017 ha autorizzato un nuovo medicinale per effettuare questo tipo di terapia genica [[il principio attivo è il voretigene neparvovec]], di cui potrebbero beneficiare 1000-2000 persone solo negli Usa.
I trucchi per sostituire il gene difettoso
È stato effettuato negli Stati Uniti uno studio triennale su 31 persone con distrofie retiniche, coinvolgendo anche bambini piccoli, presso l’Università dello Iowa e l’Ospedale pediatrico di Philadelphia. Da un lato la diagnosi è stata formulata ricorrendo a test empirici, dall’altro è stato possibile verificare l’eleggibilità dei pazienti ricorrendo a un test molecolare che evidenziasse la presenza di una mutazione dell’RPE65.

Per trasportare il nuovo gene umano RPE65 fino all’epitelio pigmentato retinico [[strato che garantisce il nutrimento e il supporto alle cellule fotosensibili]] si è fatto ricorso a una sorta di “cavallo di Troia”: un vettore virale (adenovirus, il virus del raffreddore svuotato del suo contenuto genetico nocivo) capace di infettare rapidamente molte cellule: grazie a speciali “forbici molecolari” la porzione “malata” del DNA è poi stata sostituita con un gene sano. Le cellule retiniche trattate hanno prodotto, quindi, una proteina normale in grado di convertire correttamente la luce in impulsi retinici bioelettrici che, viaggiando attraverso il nervo ottico, arrivano alla corteccia cerebrale, ripristinando quindi la visione perduta.
Le iniezioni hanno coinvolto circa un quinto della superficie retinica. Ora si proseguirà comunque la sperimentazione – che si è già svolta dal 2012 al 2015 – fino a luglio del 2029, soprattutto per garantire un follow-up adeguato, ossia per verificare che il trattamento perduri nel tempo e, se necessario, perfezionarlo.
Lo studio che ha valutato la sicurezza e l’efficacia del farmaco in persone affette da amaurosi congenita di Leber è stato pubblicato dalla rivista scientifica The Lancet.
Fonti principali: FDA, Clinical Trials, The Lancet 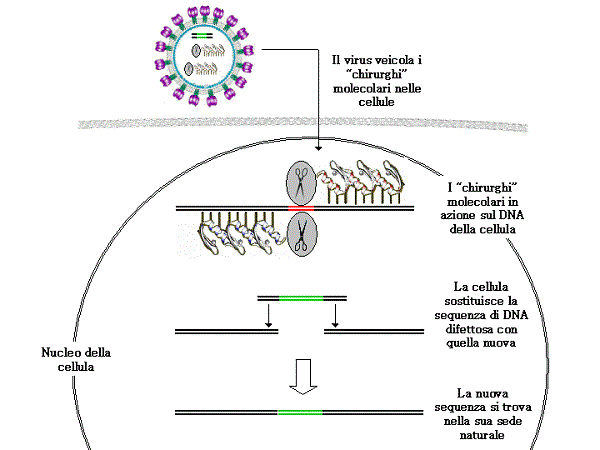









 La maggior parte dei traumi oculari sono evitabili. La prevenzione è d’obbligo soprattutto durante i festeggiamenti (in casa o fuori): bisogna stare attenti ai possibili danni fisici e, in particolare, quelli agli occhi. Si tratta, infatti, della terza parte del corpo a subire più traumi dopo le mani e i piedi. Quando si stappa lo spumante, lo champagne o il vino frizzante oppure quando si esplodono petardi e fuochi d’artificio si corrono diversi rischi da non sottovalutare mai.
La maggior parte dei traumi oculari sono evitabili. La prevenzione è d’obbligo soprattutto durante i festeggiamenti (in casa o fuori): bisogna stare attenti ai possibili danni fisici e, in particolare, quelli agli occhi. Si tratta, infatti, della terza parte del corpo a subire più traumi dopo le mani e i piedi. Quando si stappa lo spumante, lo champagne o il vino frizzante oppure quando si esplodono petardi e fuochi d’artificio si corrono diversi rischi da non sottovalutare mai.











 I cittadini vogliono curarsi nel servizio sanitario pubblico, ma fanno i conti con liste d’attesa spesso lunghe, spese per i ticket e i farmaci nonché con un’assistenza territoriale che, più del passato, mostra i suoi limiti. Tutto ciò viene analizzato nel XX Rapporto PIT Salute di Cittadinanzattiva-Tribunale per i diritti del malato – dal titolo “Sanità pubblica: prima scelta, ma a caro prezzo” –, presentato il 13 dicembre 2017 a Roma. La maglia nera per le liste d’attesa va a oculistica. Infatti chi si lamenta con Cittadinanzattiva di tempi troppo lunghi aspetta mediamente 6 mesi.
I cittadini vogliono curarsi nel servizio sanitario pubblico, ma fanno i conti con liste d’attesa spesso lunghe, spese per i ticket e i farmaci nonché con un’assistenza territoriale che, più del passato, mostra i suoi limiti. Tutto ciò viene analizzato nel XX Rapporto PIT Salute di Cittadinanzattiva-Tribunale per i diritti del malato – dal titolo “Sanità pubblica: prima scelta, ma a caro prezzo” –, presentato il 13 dicembre 2017 a Roma. La maglia nera per le liste d’attesa va a oculistica. Infatti chi si lamenta con Cittadinanzattiva di tempi troppo lunghi aspetta mediamente 6 mesi. Il 37,4% denuncia i costi elevati e gli aumenti relativi ai ticket per la diagnostica e la specialistica, mentre il 31% esprime disagio rispetto ai casi di mancata esenzione dal ticket (in aumento).
Il 37,4% denuncia i costi elevati e gli aumenti relativi ai ticket per la diagnostica e la specialistica, mentre il 31% esprime disagio rispetto ai casi di mancata esenzione dal ticket (in aumento).























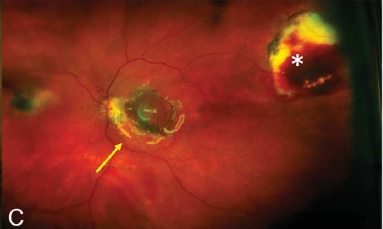
 Non solo la maculopatia miopica
Non solo la maculopatia miopica 




 A studiare la correlazione tra diabete e stili di vita c’è da qualche tempo un gruppo di esperti dell’Health City Institute, che lavorano in particolare sull’influenza degli ambienti urbani: il 7 dicembre hanno fatto il punto a Roma
A studiare la correlazione tra diabete e stili di vita c’è da qualche tempo un gruppo di esperti dell’Health City Institute, che lavorano in particolare sull’influenza degli ambienti urbani: il 7 dicembre hanno fatto il punto a Roma 



